Bioloģiskā, kas pazīstams arī kā bioloģiskās zāles vai bioloģisko faktoru, ir testi, profilaksei un terapijas, kas tika izstrādāti un tiek ražoti, izmantojot bioloģiskos procesus, izmantojot cilvēka, dzīvnieku vai mikroorganismu avotus. Tas atšķirībā no farmaceitiskajiem medikamentiem, kas ražoti no ķīmiskiem procesiem.
Bioloģiskajos produktos, piemēram, cukurā, olbaltumvielās, nukleīnskābēs, šūnās, asinīs vai audos, tiek izmantots daudzu vielu daudzums, kas iegūti no cilvēkiem, dzīvniekiem vai mikroorganismiem.
Izmantojot biotehnoloģiju, tie ir apvienoti vai apstrādāti, lai radītu vielas, kas var palīdzēt mums diagnosticēt, ārstēt, pārvaldītu vai izārstēt slimības un nosacījumiem.
Starp pirmajiem bioloģiskajiem aģentiem bija insulīnu, kas tās ātrāk veidā tika iegūta no dzīvniekiem. Mūsdienu insulīna produkti, visticamāk, ir rekombinantās DNS, atšķirīgas pieejas rezultāts, taču tie joprojām ir bioloģiski raksturīgi.
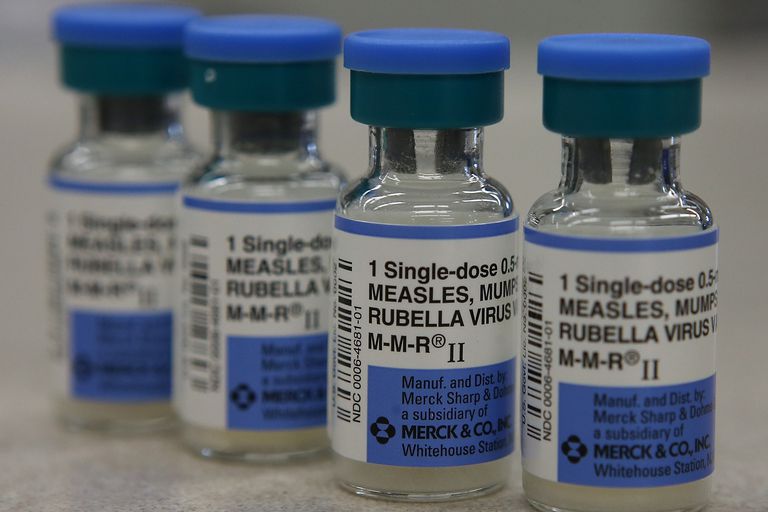
Vakcīnas ir bioloģiskas vielas, kuras ir pieejamas gadsimtiem ilgi. Tie tiek veidoti, izmantojot vīrusa komponentu vai baktērijas, kas izraisa slimības novēršanu. Tas var būt nogalināts vai mīksts dīgļa celms, vai arī tas var būt attīrīts proteīns, cukurs vai cita dīgļa sastāvdaļa.
Atklājot kādu personu šim preparātam, kas iegūts no attiecīgā vīrusa vai baktērijām, pirms tie saslimst, organisms reaģē, izveidojot antivielas pret šo slimību. Vēlāk, ja tas ir pakļauts, pacients neizraisīs slimību.
process ir viss bioloģiskais.
citi pazīstami testi un terapijas ir arī bioloģiskas. Asins produkti, ko izmanto asins pārliešanai, daudz alerģiju testus un kadri, hormonālās terapijas, piemēram, tās, ko izmanto, lai ārstētu simptomus menopauzes, un cilmes šūnu terapiju izmanto transplantācijai vai attīstībai citu bioloģisko faktoru visi tiek uzskatīti bioloģiska.
Bioloģijas saraksts
Sastādīts no vairākiem resursiem, šeit ir galvenais bioloģisko vielu saraksts:
- vakcīnas
- insulīni
- interleikīni
- cilvēka augšanas hormoni
- hormonu terapijas līdzekļi, piemēram, estrogēna vai testosterona izmantošana
- testi, lai pārbaudītu iespējamos asins donorus HIV vai citām infekcijas aģenti
- asins un asins produktu pārliešana
- asinīm un asins produktiem, kurus izmanto ražošanā ar citiem produktiem
- izmanto, lai attīstītu gan alerģijas testus un alerģijas šāvienu bioloģiski ekstraktus
- cilvēka šūnām un audiem transplantācijai izmantotie (piemēram, cīpslas, saites un kaulu)
- gēns (DNS) terapija (skatīt zemāk *)
- šūnu terapijas (skatīt zemāk *)
Katrs no tiem tiek pārdots ar zīmolu, kas var būt vairāk atpazīstams, piemēram Avastin, Herceptin, Enbrel, Epotin, Remicade, Humira vai Avonex.
Bioloģiskā nav, stingri noteiktos Generic ekvivalenti
Atšķirībā vecāki ķīmiskā sastāva narkotikām, lielākā daļa bioloģiska nav ko strikti definēta kā vispārīgiem ekvivalentiem. FDA definē patentbrīvos medikamentus kā tādas pašas aktīvās sastāvdaļas kā zīmola nosaukumu. Ne tikai to, bet arī tie ir bioloģiski līdzvērtīgi – tiem ir tāda pati zāļu forma, izturība, kvalitāte un sniegums. Tā vietā bioloģiskajai vielai ir biosimilāri, kas likumā tika noteikti 2009. gadā.
Biosimilars
Biosimilars ir FDA apstiprinātas zāles, kurām nav klīniski nozīmīgu atšķirību no sākotnējā zīmola bioloģiskā aģenta.
Tiem jābūt tikpat drošiem un tikpat efektīviem un jāstrādā tāpat kā atsauces līdzeklis. Zāļu sauc par savstarpēji aizstājamu, ja tā atbilst biosimilaritātes standartam, un tai jābūt iespējai pārslēgties no oriģinālā produkta bez riska palielināšanās.
Amerikas Savienotajās Valstīs tika ierobežota bioloģiski līdzīgu zāļu recepte līdz 2010. gada Likumam par pieejamu aprūpi. Līdz ar 2009. gada Bioloģisko cenu sacensību un jauninājumu akta (BCPI) un 2010. gada Likumu par pacientu aizsardzību un pieejamu aprūpi, Bioloģiskie produkti ir racionalizēti licencēšanas ceļā caur FDA.
Ar izmaiņām tiesību aktos Amerikas Savienotajās Valstīs būs pieejams arvien vairāk bioloģiski līdzīgu un savstarpēji aizstājamu narkotiku.
Pirms 2009. gada daudzas grupas lobēja, lai mudinātu FDA uzsākt biosimilāru ražošanu vai vecāku bioloģisko materiālu turpmāku versiju, lai ietaupītu veselības aprūpes sistēmas naudu. Piemēram, firmas insulīns un insulīna tipa produkti var maksāt no $ 150 līdz $ 1000 mēnesī. Turpmāka ekvivalents var maksāt tikai 25 ASV dolārus mēnesī. Ja reizina ar to cilvēku skaitu, kam vajadzīgas šāda veida ārstēšana, jūs varat redzēt, kā šo turpmāko bioloģisko līdzekļu apstiprināšana varētu ietaupīt sistēmas miljardus.
Lielie bioloģiskie ražotāji lobēja pret biosimilāru attīstību un ražošanu, jo viņi nevēlējās sacensties ar lētākām, bet efektīvām ārstēšanas metodēm (ievērojiet naudu). Viņi minēja drošības problēmas attīstības procesā un pierādījumu trūkumu, ka šīs zāles būtu tikpat efektīvas kā oriģināli.

